Última Atualização 25/ 3/ 2010
em Inglês/ em Esperanto/ em Português
Reações químicas de oxidação e redução ou de oxirredução ou redox podem ocorrer espontaneamente quando houver espécie química material capaz de doar elétron em contato com espécie química capaz de receber elétron. A espécie química que doa elétron é denominada redutor e a espécie química que recebe elétron denomina-se oxidante. Quando se esgota o redutor a reação para. A reação também para quando se esgota o oxidante. Porém tornará a se restabelecer a reação de redox sempre que o componente que se esgotou for suprido novamente. A espécie química redutora pode doar mais de um elétron contanto que haja oxidante para receber todos os elétrons e a espécie química oxidante poderá receber mais de um elétron se houver redutor que os forneça.
O estudo detalhado do tema acima emprega convenções e metodologia universalmente aceita.
Quando o redutor e o oxidante citados acima estiverem em recipientes separados mas conectados por condutor elétrico e por uma ponte salina que permite a eletroneutralidade do meio, a reação química de oxidação e redução também ocorrerá. Neste caso a migração do elétron doado pelo redutor a partir de um recipiente é conduzida pelo condutor até o outro recipiente onde se encontra o oxidante que recebe o elétron. A migração dos elétrons pelo condutor é denominada de corrente elétrica. Tal montagem experimental constitui uma pilha ou bateria ou célula galvânica. Em condições adequadas a corrente elétrica possibilita acionar um aparelho eletrônico para calcular, um aparelho para emitir um som, mover um motor ou fazer com que uma lâmpada brilhe. Se uma corrente elétrica for injetada em oposição em condições adequadas o funcionamento da pilha será inibido ou completamente bloqueado ou poderá recarregar a pilha ou cela eletrolítica. Durante o recarregamento procede a síntese da espécie química que foi consumida na célula galvânica.
O resumo acima fornece indícios rudimentares para o entendimento de reações redox que ocorrem nos seres vivos. A natureza dos seres vivos é caracterizada por grande organização de consumo de espécies químicas, síntese de espécies químicas em solução ou em recipientes separados por membranas seletivas, receptores e doadores de elétrons, energias consumidas e energias liberadas em dosagens bem reguladas, a fim de permitir a manifestação física do próprio ser. Quando as condições materiais declinam devido a fatores externos, a organização deficiente diminui ou bloqueia a manifestação física do ser vivente. Suprimento dosado de energia e substituição de componentes materiais em tempo hábil podem restabelecer a condição de manifestação física do ser. Por outro lado, quando o próprio ser vivente entra em desequilíbrio, ele descontrola e desorganiza as condições necessárias para manter a sua manifestação física e ela cessa. O ser vivente voltará a apresentar manifestação física quando ele estiver em condições de reconhecer e gerenciar um outro sistema organizado e funcional quando disponível.
Exemplos de reações de oxidação e redução
a) Zinco metálico reduz íons de cobre a cobre metálico.
![]()
b) Íon dicromato oxida um álcool a uma cetona.
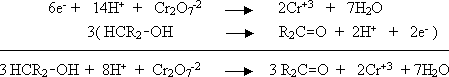
c) Nicotinamida adenina dinucleotídeo ( NAD+ ) metaboliza etanol a aldeido acético. As fórmulas estruturais do NAD+ e do NADH são selecionaveis de acordo com o clique no botão coorespondente à figura desejada.
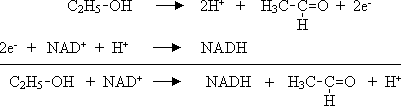
Referências
Qualquer bom livro de química geral, de química orgânica e de bioquímica.
Tabela de temas
| Apresentação |